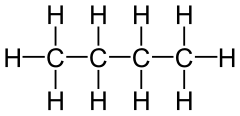
Бутан (C4H10) – це хімічна сполука, класу алканів є газоподібною речовиною за кімнатної температури та атмосферного тиску. Бутан складається з чотирьох атомів вуглецю та десяти атомів водню.
Важливою рисою бутану є його здатність до сжиження під тиском, що дозволяє транспортувати та зберігати його у рідкому стані.
Фізичні властивості бутану
Основні фізичні властивості бутану (C4H10) включають:
- Агрегатний стан: Бутан є газоподібною речовиною за кімнатної температури та атмосферного тиску. Однак, при достатньо низькій температурі і під певним тиском, він може перетворитися у рідкий стан.
- Колір та запах: Бутан є безбарвним та без запаху.
- Точка кипіння: Точка кипіння бутану становить близько -0,5 градусів Цельсія (-0,42 градусів Фаренгейта).
- Точка плавлення: C4H10 не має точки плавлення, оскільки він перетворюється з газоподібного стану на рідкий стан без переходу через твердий стан.
- Густина: Густина бутану у газоподібному стані становить близько 2,48 г/л.
- Розчинність: Бутан не розчиняється у воді, але може бути розчиненим в органічних розчинниках, таких як етанол та ефіри.
- Тиск насиченої пари: Насичений пар бутану має високий тиск. При нормальних умовах температури і тиску, цей тиск становить близько 2,4 атмосфери.
Ці характеристики можуть змінюватися залежно від умов температури та тиску, під якими знаходиться бутан.
Хімічні властивості бутану
Бутан (C4H10) має деякі хімічні властивості, які варто враховувати:
- Горіння: Бутан – це легкозаймиста речовина, яка сприймає горіння в присутності кисню. Під час горіння бутан окислюється до вуглекислого газу (CO2) та води (H2O) з виділенням енергії.
- Реакція з киснем: C4H10 може піддаватися повільному окисненню у присутності кисню або повітря. Це може призвести до утворення оксидів вуглецю (COx) та оксидів азоту (NOx).
- Реакція з галогенами: Бутан може взаємодіяти з галогенами (наприклад, хлором або бромом) при підходящих умовах, утворюючи галогеновані похідні бутану. Наприклад, хлорація бутану може привести до утворення 1,1-дихлорбутану або 1,4-дихлорбутану, залежно від умов реакції.
- Реакція з кислотами: C4H10, як алкан, не реагує з кислотами, такими як сірчана кислота або хлороводнева кислота, за звичайних умов. Однак, високотемпературна реакція бутану з киснем може призводити до утворення вуглекислоти.
Ці хімічні властивості бутану використовуються в різних процесах і промислових додатках, таких як зварювання, паливні системи та хімічна синтез. Проте, важливо дотримуватися правил безпеки при роботі з бутаном, оскільки він є займистою речовиною.
Використання бутану
Бутан (C4H10) має широке використання у різних галузях.
Деякі з основних способів використання бутану включають:
- Побутове використання: C4H10 є популярним джерелом палива для газових плит, газових камінів, газових грилів та інших побутових приладів. Він є зручним і легкодоступним джерелом енергії для приготування їжі та опалення приміщень.
- Транспорт: Бутан використовується як альтернативне паливо для автомобілів. У деяких країнах встановлюються газові системи, які дозволяють перетворити бензинові двигуни на газові. Це може бути економічно вигідним і сприяти зниженню викидів шкідливих речовин у повітря.
- Промисловість: Бутан є важливою сировиною для хімічної промисловості. Він використовується для виробництва пластиків, розчинників, лаків, аерозолів та інших хімічних продуктів. C4H10 також може бути використаний як паливо для нагрівальних систем і теплових процесів у різних галузях промисловості.
- Аерозольні продукти: Бутан використовується як пропелент у багатьох аерозольних продуктах, таких як засоби для догляду за волоссям, дезодоранти, фарби, змащувальні засоби тощо. Він дозволяє створювати стабільний тиск, який вимушує продукт виходити з контейнера у вигляді розпиленої хмари.
- Енергетика: Бутан може бути використаний як енергетичне паливо для генерування електроенергії. Це може включати використання бутану в енергетичних станціях або установку генераторів, які працюють на бутані.