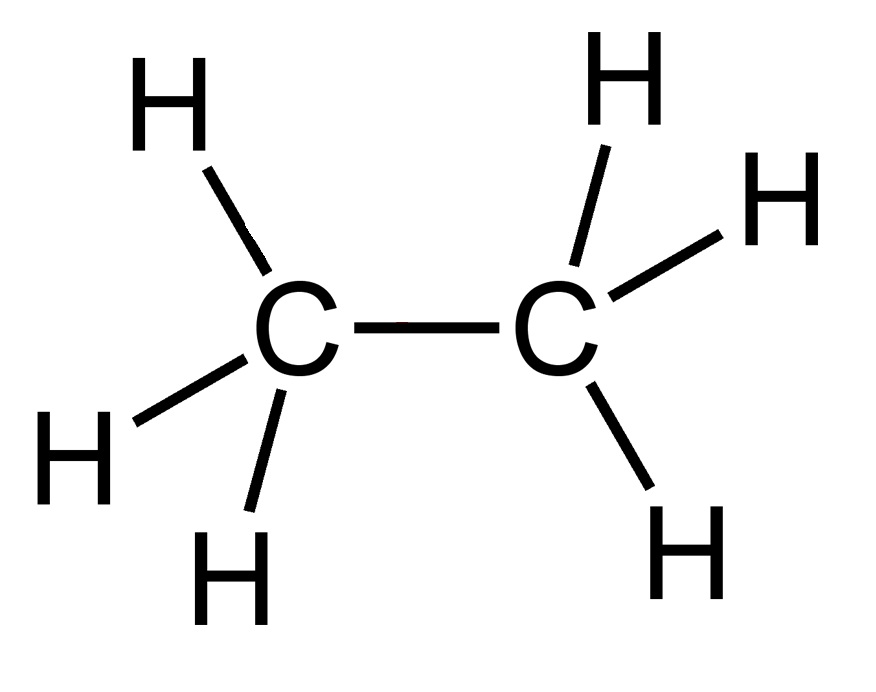
Етан (C2H6) – це органічна сполука, яка належить до класу алканів. Він складається з двох молекул водню та шести атомів вуглецю. Етан є одним з простих та найбільш поширених представників алканів.
Етан може бути використаний як паливо. Він легко горить у повітрі, утворюючи вуглекислий газ та воду. Етан також використовується в якості сировини для отримання етену (етилену), який в свою чергу використовується у багатьох хімічних процесах та як мономер для синтезу поліетилену, який є одним з найпоширеніших пластиків.
Фізичні властивості етану
- Молярна маса: 30,07 г/моль
- Температура кипіння: -88,6 °C
- Температура плавлення: -182,8 °C
- Густина: 0,544 г/см³ (газова стан при 25 °C та 1 атмосфері)
- Безбарвний та беззапаховий газ при нормальних умовах
Хімічні властивості етану
Етан (C2H6) має наступні хімічні властивості:
- Горіння: Етан є досить легкозаймистим газом. При спалюванні у наявності достатньої кількості кисню утворюється вуглекислий газ (CO2) та вода (H2O). Реакція горіння етану може бути представлена наступним чином:
C2H6 + 3.5O2 -> 2CO2 + 3H2O
- Галогенування: Етан може реагувати з галогенами, такими як хлор (Cl2) чи бром (Br2), за утворення галогенетанів. Наприклад, реакція етану з хлором може мати такий вигляд:
C2H6 + Cl2 -> C2H5Cl + HCl
- Окиснення: Етан може бути окиснений до утворення вуглекислого газу та води. Наприклад, при нагріванні етану з киснем (O2) в присутності каталізатора, такого як платина (Pt), може відбутися наступна реакція:
2C2H6 + 7O2 -> 4CO2 + 6H2O
- Гідрогеноліз: Етан може пройти реакцію гідрогенолізу, внаслідок якої здійснюється розрив зв’язку між вуглецевими атомами, замінюючи їх воднем. Наприклад, реакція гідрогенолізу етану може мати такий вигляд:
C2H6 + H2 -> 2CH4
Це лише декілька прикладів хімічних властивостей етану. Як багато інших органічних сполук, він може утворювати різні типи реакцій залежно від умов та реагентів, що застосовуються.
Отримання
Етан (C2H6) можна отримати за допомогою різних методів.
Ось декілька способів отримання етану:
- Кракування нафти: Нафту, яка є сумішшю різних вуглеводневих сполук, можна піддати процесу кракування (розщеплення) для отримання легких вуглеводнів, включаючи етан. Цей процес відбувається за високих температур та тиску.
- Реформінг природного газу: Природний газ, який складається в основному з метану, можна піддати процесу реформінгу, де він розщеплюється на більш важкі вуглеводні, включаючи етан.
- Переробка біомаси: Деякі види біомаси, такі як деревина або багас, можуть бути перероблені в процесі піролізу або газифікації, що дозволяє отримувати різні газові продукти, включаючи C2H6.
- Реакція заліза з метаном: Метан (CH4) може реагувати з гарячим металевим каталізатором, таким як залізо (Fe), за утворення етану. Ця реакція відбувається при високих температурах.
- Гідрогеноліз: C2H6 може бути отриманий шляхом гідрогенолізування більш важких вуглеводнів, таких як пропан або бутан. Цей процес вимагає наявності водню (H2) та каталізатора.
Це лише кілька способів отримання етану. Вибір конкретного методу залежить від доступної сировини, економічної ефективності та потреб споживачів.
Застосування
Етан (C2H6) має різноманітні застосування в різних галузях.
Ось декілька основних застосувань етану:
- Паливо: Етан використовується як паливо для домашнього використання, комерційних та промислових систем опалення. Він може бути змішаний з природним газом або використовуватись окремо.
- Сировина для хімічної промисловості: C2H6 є важливою сировиною для виробництва різних хімічних сполук. Він використовується як основна сировина для отримання етену (етилену), який є ключовим компонентом у виробництві поліетилену, одного з найпоширеніших пластиків. Також етан використовується для виробництва етанолу, хлоретану, етиленгліколю та інших хімічних сполук.
- Виробництво електроенергії: Етан може бути використаний у газових турбінах або спалюватись у генераторах електроенергії для виробництва електричної енергії.
- Аерозольні пропеленти: Етан може бути використаний як компонент у складі аерозольних пропелентів, що використовуються в косметиці, лікарських препаратах та інших продуктах.
- Застосування у нафтогазовій промисловості: C2H6 використовується як розчинник для виділення та очищення природного газу та нафтопродуктів. Він може також бути доданий до природного газу для підвищення його енергетичної цінності.
- Холодоагент: C2H6 може бути використаний як холодоагент у холодильних системах та кондиціонерах.