Ізобарний процес — це термодинамічний процес, при якому тиск газу залишається постійним.
Прикладом ізобаричного процесу може бути нагрівання води у відкритій посудині, або розширення газу у циліндрі з поршнем, який може вільно рухатись. В обох випадках тиск дорівнює атмосферному.
- Тиск (P): Залишається постійним
- Об’єм (V): Може змінюватися
- Температура (T): Може змінюватися
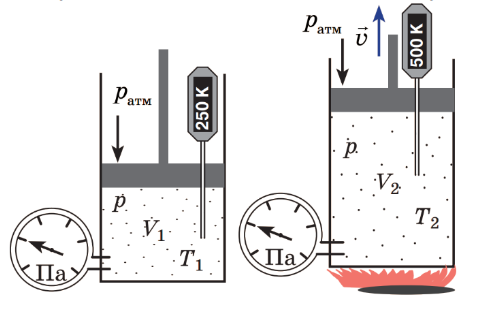
При збільшенні температури газу збільшується кінетична енергія руху молекул, а отже і швидкість руху молекул. Однак сталість тиску означає, що при цьому зменшується кількість молекул в одиниці об’єму речовини. При чому зменшення концентрації молекул пропорційна до збільшення кінетичної енергії їх руху.
Ізобарний процес описується законом Ґей-Люссака.
Закон Ґей-Люссака
Для даного газу деякої маси відношення об’єму газу до температури є незмінним, якщо тиск газу не змінюється.
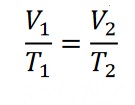
Цей закон експериментально встановив у 1802 р. французький фізик Жозеф Луї Ґей-Люссак (1778 –1850)