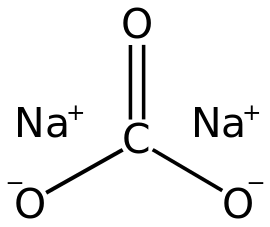
Карбонат натрію (Na2CO3) також відомий як кальцинована сода.
Безбарвні кристали або білий порошок, гігроскопічна, добре розчинна у воді. Розчини мають сильнолужну реакцію.
Він малотоксичний і належить до III класу небезпеки.
| Молярна маса | 105,99 г/моль |
| Молекулярна маса | 106 а.о.м. |
| Густина | 2,53 г/см³ |
| Тпл | 852 °C |
| Ткип | 1600 °C |
| Кислотність (pKa) | 10.33 |
| Основність (pKb) | 4.67 |
У водному розчині Na2CO3 гідролізується, що зумовлює лужну реакцію середовища. Рівняння гідролізу (в іонній формі):
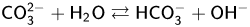
Взаємодія з кислотами
Перша константа дисоціації вугільної кислоти дорівнює 4,5⋅10−7. Усі кислоти, сильніші, ніж вугільна, витісняють їх у реакції з карбонатом натрію. Так як вугільна кислота вкрай нестійка, вона відразу розкладається на воду і вуглекислий газ:
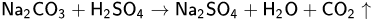
Застосування
Карбонат натрію, також відомий як кальцинована сода, використовується в багатьох галузях промисловості, включаючи:
- Хімічна промисловість: Na2CO3 використовується як сировина для виробництва інших хімічних речовин, таких як каустична сода (NaOH), гідроксид натрію (NaOH) та скло.
- Скловиробництво: Карбонат натрію використовується як флюс при виготовленні скла, що робить його більш міцним і стійким до хімічних впливів.
- Паперова промисловість: Na2CO3 використовується в процесі виробництва паперу для видалення деревини.