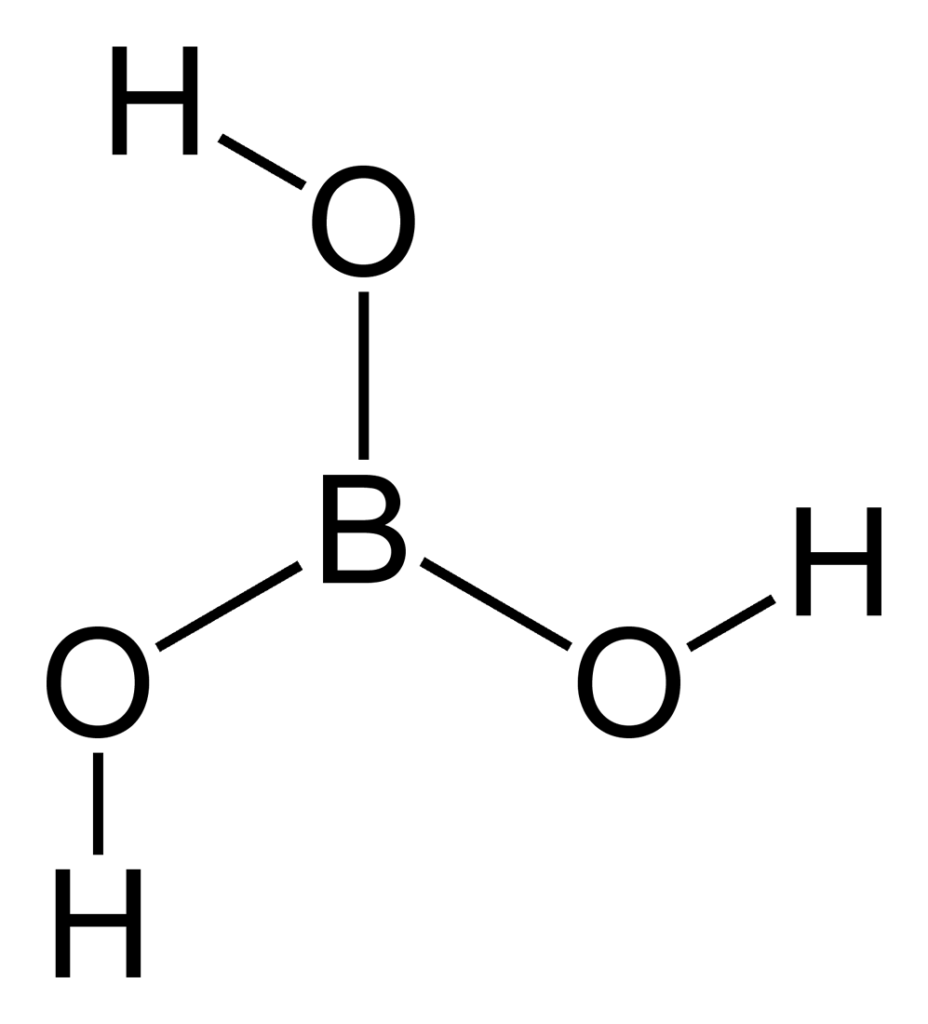
Борна кислота (H3BO3) — це слабка моноосновна кислота, яка складається з трьох молекул води і молекули бору.
Інші назви: ортоборна, ортоборатна, боратна кислота
Хімічні властивості борної кислоти
Борна кислота (H3BO3) має наступні хімічні властивості:
- Реакція з лугами: Борна кислота взаємодіє з лугами, утворюючи боратні солі. Наприклад, реакція з гідроксидом натрію (NaOH) може мати наступний вигляд: H3BO3 + NaOH → Na[B(OH)4]
- Дисоціація: У водних розчинах H3BO3 слабо дисоціює, утворюючи іони водню (H+) і іони борату (BO3-). Дисоціація відбувається згідно з рівнянням: H3BO3 ⇌ H+ + H2BO3-
- Амфотерність: H3BO3 має амфотерні властивості, тобто вона може взаємодіяти як з лугами, так і з кислотами. Вона може реагувати з основами, утворюючи боратні солі, і з кислотами, утворюючи боратні естери.
- Окиснювальні властивості: Високі температури та концентровані розчини борної кислоти можуть виявляти окислювальну активність.
- Утворення комплексних сполук: H3BO3 може утворювати комплексні сполуки з деякими іонами, наприклад, з металами, які мають високу афінітет до бору.
- Властивості гідрату: Борна кислота існує у вигляді гідрату, в якому молекули кислоти зв’язані з молекулами води. Наприклад, пентагідрат борної кислоти (H3BO3·5H2O) є одним з поширених гідратів.
Важливо враховувати, що борна кислота може бути слабкою, але все ж кислотою, тому потрібно дотримуватися відповідних заходів безпеки при роботі.
Отримання
Борну кислоту (H3BO3) можна отримати декількома способами. Один з них – це окиснення борної складової природи, такої як боракс (Na2B4O7·10H2O), або борангідрату (BH3·THF), киснем або кисневмісними газами, наприклад, повітрям.
Ось загальна реакція:
2 B2O3 + 3 O2 → 2 H3BO3
У цій реакції борна складова, така як боракс або борангідрат, окислюється киснем або кисневмісними газами, утворюючи борну кислоту.
Інший метод отримання борної кислоти включає реакцію борангідрату (BH3·THF) з холоридом водню (HCl). Реакція може мати наступний вигляд:
BH3·THF + 3 HCl → B(OH)3 + 3 THF + H2Cl2
У цій реакції борангідрат реагує з холоридом водню, утворюючи борну кислоту, тетрагідрофуран (THF) і дихлорид водню (H2Cl2).
Варто підкреслити, що отримання борної кислоти може вимагати використання спеціального обладнання та дотримання певних заходів безпеки
Застосування
Борна кислота (H3BO3) має широкий спектр застосувань у різних галузях.
Ось деякі з них:
- Виробництво скла: Борна кислота є важливим складником у виробництві скла. Вона використовується як плавильний агент, що знижує температуру плавлення скляної маси і покращує її хімічну стійкість.
- Сільське господарство: H3BO3 використовується як мікроелементне добриво для рослин. Бор є необхідним для правильного розвитку рослин, а його додавання у вигляді борної кислоти допомагає уникнути борування ґрунту.
- Вогнезахисні матеріали: Борна кислота використовується як складник у вогнезахисних матеріалах. Вона здатна запобігати поширенню вогню і використовується в покриттях, піноутворювачах та інших вогнезахисних матеріалах.
- Хімічна промисловість: Борна кислота використовується як каталізатор або проміжний продукт у виробництві різних хімічних речовин, таких як полімери, синтетичні смоли та фарби.
- Медична і косметична промисловість: H3BO3 використовується в деяких медичних і косметичних продуктах, наприклад, як консервант, антибактеріальний агент або регулятор pH.
- Аналітична хімія: Борна кислота використовується як реагент у хімічних аналітичних методах для визначення наявності та кількості деяких речовин, таких як феноли, аміносполуки та металеві катіони.